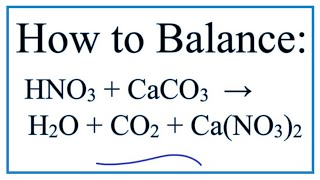
CaCO3 + HNO3 → Ca(NO3)2 + CO2 + H2O được biên soạn gửi tới bạn đọc là phương trình phản ứng CaCO3 tác dụng HNO3 sau phản ứng có khí không màu thoát ra. Mời các bạn tham khảo chi tiết nội dung phương trình dưới đây.
>> Mời các bạn tham khảo thêm một số phương trình liên quan
- Ca(OH)2 + H2SO4 ⟶ CaSO4 + H2O
- CaCO3 → CaO + CO2
- CaCO3 + HCl → CaCl2 + CO2 + H2O
- CaCO3 + HNO3 → Ca(NO3)2 + CO2 + H2O
- CaCO3 + CO2 + H2O → Ca(HCO3)2
- CaOCl2 + HCl → CaCl2 + Cl2 + H2O
- CaOCl2 → CaCl2 + O2
1. Phương trình phản ứng CaCO3 ra CO2
2. Điều kiện phản ứng xảy ra CaCO3+ HNO3
Nhiệt độ thường
3. Khi có CaCO3 tác dụng HNO3 có hiện tượng
Chất rắn màu trắng CaCO3 tan dần và sinh ra khí CO2 làm sủi bọt dung dịch
4. Tính chất hóa học của CaCO3
Mang đầy đủ tính chất hóa học của muối:
Tác dụng với axit mạnh:
CaCO3 + 2HCl → CaCl2 + H2O + CO2
Kém bền với nhiệt:
CaCO3  CaO + CO2
CaO + CO2
CaCO3 tan dần trong nước có hòa tan khí CO2.
CaCO3 + CO2 + H2O ⇆ Ca(HCO3)2
→ khi đung nóng:
Ca(HCO3)2  CaCO3↓ + CO2 + H2O
CaCO3↓ + CO2 + H2O
5. Bài tập vận dụng liên quan
Câu 1. Khi cho chất rắn CaCO3 tác dụng với dung dịch axit HNO3 xảy ra hiện tượng gì
A. Xuất hiện kết tủa trắng
B. Xuất hiện khí
C. chất rắn màu trắng tan, sinh ra khí CO2
D. Không thấy hiện tượng gì
Câu 2. Phản ứng nào dưới đây không xảy ra
A. CO2 + dung dịch Na2CO3 →
B. Fe2O3 + C →
C. CaCO3 + HNO3 →
D. CO2 + H2O + BaSO4 →
Câu 3. Cho 10 gam CaCO3 tác dụng hoàn toàn với dung dịch HNO3 loãng dư thu được V lít khí CO2 (đktc). Giá trị V của là
A. 5,60.
B. 2,24.
C. 3,36.
D. 4,48.
Câu 4. Cho hổn hợp C và S vào dung dịch HNO3 đặc thu được hổn hợp khí X và dung dịch Y. Thành phần của X là
A. SO2 và NO2.
B. CO2 và SO2.
C. CO2 và NO2.
D. SO2 và NO.
Câu 5. Trong các cặp chất cho dưới đây, cặp chất nào có thể cùng tồn tại trong một dung dịch?
A. NaCl và CuSO4.
B. NH3 và AgNO3.
C. CaCO3 và HNO3.
D. NaHSO4 và NaHCO3.
Câu 6. Cho 2,7 gam hỗn hợp gồm Cu, Mg, Al tác dụng với dung dịch HNO3 dư, thu được 2,24 lít (đktc) hỗn hợp khí NO và NO2 có tỉ khối so với hiđro bằng 20. Tổng khối lượng muối nitrat sinh ra là :
A. 66,75 gam.
B. 13,55 gam.
C. 6,775 gam.
D. 3,335 gam.
Câu 7. Axít HNO3 đặc nóng phản ứng được với nhóm chất nào sau đây:
A. Mg(OH)2, CuO, NH3, CO2, Au, C, FeSO4
B. Mg(OH)2, CuO, NH3, H2SO4, Mg, C, Fe2O3, Fe3O4
C. Mg(OH)2, CuO, NH3, Pt, Ag, C, Fe2O3, Fe3O4
D. Mg(OH)2, CuO, NH3, Ag, C, Fe2O3, Fe3O4
Câu 8. Cho các chất sau: Fe(OH)3, Fe3O4, FeSO4, Fe(NO3)2. Số chất tác dụng với dung dịch HCl là
A. 4.
B. 2.
C. 3.
D. 1.
Câu 9. Tiến hành các thí nghiệm sau:
(a) Điện phân NaCl nóng chảy.
(b) Cho dung dịch Fe(NO3)2 vào dung dịch AgNO3 dư.
(c) Nhiệt phân hoàn toàn CaCO3.
(d) Cho kim loại Na vào dung dịch CuSO4 dư.
(e) Dẫn khí H2 dư đi qua bột CuO nung nóng.
Sau khi các phản ứng kết thúc, số thí nghiệm thu được kim loại là
A. 1.
B. 4.
C. 3.
D. 2.
Câu 10. Dãy các chất đều tác dụng với dung dịch Ca(OH)2 là:
A. Ba(NO3)2, Mg(NO3)2, HCl, CO2, Na2CO3.
B. Mg(NO3)2, HCl, BaCO3, NaHCO3, Na2CO3.
C. NaHCO3, Na2CO3, Mg(NO3)2, Ba(NO3)2.
D. NaHCO3, Na2CO3, CO2, Mg(NO3)2, HCl.
………………………………….
>> Mời các bạn tham khảo một số tài liệu liên quan:
- Kim loại tác dụng với dung dịch axit
- Phương pháp giải bài tập kim loại
Trên đây VnDoc.com vừa giới thiệu tới các bạn phương trình hóa học CaCO3 + HNO3 → Ca(NO3)2 + CO2 + H2O, mong rằng qua bài viết này các bạn có thể học tập tốt hơn môn Hóa lớp 12. Mời các bạn cùng tham khảo thêm các môn Ngữ văn 12, Tiếng Anh 12, Thi thpt Quốc gia môn Toán, Thi THPT Quốc gia môn Vật Lý,….
Chúc các bạn học tập tốt.