Bài viết này chúng ta cùng tìm hiểu về Hiện tượng điện li là gì: khi axit bazo và muối tan trong nước xảy ra hiện tượng gì? Phản ứng xảy ra trong dung dịch nước có đặc điểm gì? Phân loại chất điện ly mạnh chất điện ly yếu bằng cách nào?
I. Hiện tượng điện li
1. Thí nghiệm hiện tượng điện li
– Khi nối các đầu dây dẫn điện với cùng một nguồn điện, ta chỉ thấy bóng đèn ở cốc đựng dung dịch NaCl bật sáng. Vậy dung dịch NaCl dẫn điện, còn nước cất và dung dịch saccarozơ không dẫn điện.
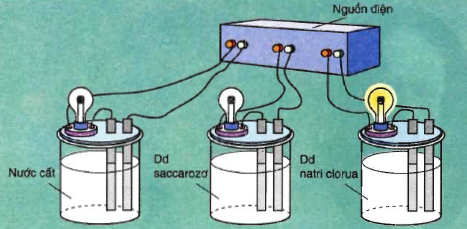
– Nếu làm các thí nghiệm tương tự, người ta thấy: NaCl rắn, khan; NaOH rắn, khan; các dung dịch ancol etylic C2H5OH , glixerol C2H5(OH)3 không dẫn điện.
– Ngược lại, các dung dịch axit, bazơ và muối đều dẫn điện.
2. Nguyên nhân tính dẫn điện của các dung dịch axit, bazơ và muối trong nước
• Ngay từ năm 1887, A-rê-ni-ut (S.Arrhenius) đã giả thiết và sau này thực nghiệm đã xác nhận rằng:
– Tính dẫn điện của các dung dịch axit, bazơ và muối là do trong dung dịch của chúng có các tiểu phân mang điện tích chuyển động tự do được gọi là các ion.
– Quá trình phân li các chất trong nước ra ion là sự điện li. Những chất tan trong nước phân li ra ion được gọi là những chất điện li .
→ Vậy axit, bazơ và muối là những chất điện li.
• Sự điện li được biểu diễn bằng phương trình điện li, ví dụ:
– Muối phân li thành cation kim loại và anion gốc axit:
NaCl → Na+ + Cl−
– Axit phân li thành cation H+ và anion gốc axit:
HCl → H+ + Cl−
– Bazơ phân li thành cation kim loại và anion hiđroxit:
NaOH → Na+ + OH−
3. Định nghĩa sự điện li
– Sự điện li là quá trình phân li thành các ion (cation, anion) khi chất tan vào nước hoặc nóng chảy.
– Chất điện li là những chất khi tan vào nước tạo thành dung dịch dẫn điện nhờ phân li thành ion.
II. Phân loại chất điện li mạnh, chất điện li yếu
1. Độ điện li
– Để biểu thị mức độ phân li ra ion của các chất điện li, ta dùng khái niệm độ điện li.
+ Độ điện li α (anpha) của một chất điện li là tỉ số giữa phân tử phân li thành ion (n) và tổng số phần tử hòa tan (n0).
+ Tỉ lệ phân tử cũng là tỉ lệ với số mol, nên αα bằng tỉ số phần nồng độ mol chất tan phân li thành Cp và tổng nồng độ mol của chất tan trong dung dịch Ct:
• Độ điện li α phụ thuộc vào:
– Bản chất của chất tan.
– Bản chất của dung môi.
– Nhiệt độ
– Nồng độ chất điện li.
2. Chất điện li mạnh và chất điện li yếu
a) Chât điện li mạnh
• Chất điện li mạnh là chất khi tan trong nước, các phân tử hoà tan đều phân li ra ion
• Những chất điện li mạnh là:
– Các axit mạnh như: HCl, HNO3, HClO4, H2SO4, …
– Các bazơ mạnh như NaOH, KOH, Ba(OH)2Ba(OH)2,… và hầu hết các muối.
• Trong phương trình điện li của chất điện li mạnh, người ta dùng một mũi tên chỉ chiều của quá trình điện li.
*Ví dụ: Na2SO4 → 2Na+ + SO42−
b) Chất điện li yếu
• Chất điện li yếu là chất khi tan trong nước chỉ có một phần số phân tử hoà tan phân li ra ion, phần còn lại vẫn tồn tại dưới dạng phân tử trong dung dịch.
• Những chất điện li yếu là:
– Các axit yếu như: CH3COOH, HClO, H2S, HF, H2SO3, …
– Các bazơ yếu như: Bi(OH)3, Mg(OH)2, …
• Trong phương trình điện li của chất điện li yếu, người ta dùng hai mũi tên ngược chiều nhau.
*Ví dụ: CH3COOH CH3COO− + H+
• Cân bằng điện li là cân bằng động. Giống như mọi cân bằng hoá học khác, cân bằng điện li cũng tuân theo nguyên lí chuyển dịch cân bằng Lơ Sa-tơ-li-ê.
B. Bài tập Sự điện li
* Bài 1 trang 7 SGK Hóa 11: Các dung dịch axit như HCl, bazơ như NaOH và muối như NaCl dẫn điện được, còn các dung dịch như ancol etylic, saccarozơ, glixerol không dẫn điện được là do nguyên nhân gì?
> Lời giải bài 1 trang 7 SGK Hóa 11
* Bài 2 trang 7 sgk hoá 11: Sự điện li, chất điện li là gì? Những loại chất nào là chất điện li? Thế nào là chất điện li mạnh, chất điện li yếu? Lấy thí dụ và viết phương trình điện li của chúng?
> Lời giải bài 2 trang 7 SGK Hóa 11
* Bài 3 trang 7 sgk hóa 11: Viết phương trình điện li của những chất sau:
a.) Các chất điện li mạnh: Ba(NO3)2 0.10 M; HNO3 0,020 M; KOH 0,010 M. Tính nồng độ mol của từng ion trong dung dịch.
b) Các chất điện li yếu HClO; HNO2.
> Lời giải bài 3 trang 7 SGK Hóa 11
* Bài 4 trang 7 sgk hóa 11: Chọn câu trả lới đúng trong các câu sau đây. Dung dịch chất điện li dẫn được điện là do:
A. Sự dịch chuyển của các electron.
B. Sự dịch chuyển của các cation.
C. Sự dịch chuyển của các phân tử hoà tan.
D. Sự dịch chuyển của cả cation và anion.
> Lời giải bài 4 trang 7 SGK Hóa 11
* Bài 5 trang 7 sgk hóa 11: Chất nào sau đây không dẫn điện được?
A. KCl rắn, khan.
B. CaCl2 nóng chảy.
C. NaOH nóng chảy.
D. HBr hoà tan trong nước.
> Lời giải bài 5 trang 7 SGK Hóa 11
