Phản ứng Mg(OH)2 + HCl → MgCl2 + H2O
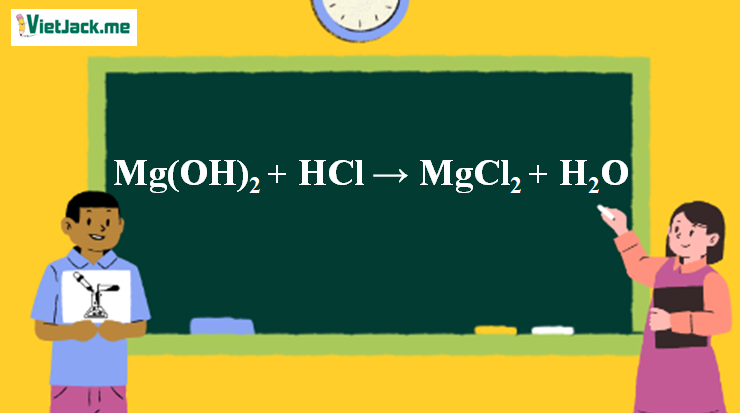
1. Phương trình phản ứng Mg(OH)2 + HCl
2. Điều kiện phương trình phản ứng xảy ra
Nhiệt độ thường
3. Hiện tượng phản ứng xảy ra
Khi cho Magie hidroxit tác dụng với dung dịch axit. Chất rắn màu trắng Magie hidroxit (Mg(OH)2) tan dần.
4. Bản chất của các chất tham gia phản ứng
4.1. Bản chất của Mg(OH)2 (Magie hidroxit)
Mg(OH)2 mang tính chất hóa học của bazo không tan tác dụng với axit như HCl, HNO3,..
4.2. Bản chất của HCl (Axit clohidric)
HCl tác dụng bazơ tạo thành muối clorua + nước.
5. Mở rộng kiến thức về Mg(OH)2
5.1. Tính chất vật lí
Là chất rắn, có màu trắng, không tan trong nước.
5.2. Tính chất hóa học
Mang tính chất hóa học của bazo không tan
Bị phân hủy bởi nhiệt:
Mg(OH)2 -to→ H2O + MgO
Tác dụng với axit:
2HNO3 + Mg(OH)2 → 2H2O + Mg(NO3)2
2HCl + Mg(OH)2 → 2H2O + MgCl2
5.3. Điều chế
– Cho muối của Magie tác dụng với dung dịch bazơ
MgCl2 + 2NaOH → Mg(OH)2 + 2NaCl
– Ở quy mô thương mại, Mg(OH)2 được sản xuất bằng cách xử lý nước biển với canxi hydroxit (Ca(OH)2). 600 m3 nước biển sản xuất được khoảng một tấn Mg(OH)2. Ca(OH)2 dễ hòa tan hơn so với Mg(OH)2, nên magiê hydroxit kết tủa thành chất rắn:
Mg2+ + Ca(OH)2 → Mg(OH)2 + Ca2+
6. Tính chất hóa học của HCl
Dung dịch axit HCl có đầy đủ tính chất hoá học của một axit mạnh.
6.1. Tác dụng chất chỉ thị
Dung dịch HCl làm quì tím hoá đỏ (nhận biết axit)
HCl → H+ + Cl-
6.2. Tác dụng với kim loại
Tác dụng với KL (đứng trước H trong dãy Bêkêtôp) tạo muối (với hóa trị thấp của kim loại) và giải phóng khí hidrô (thể hiện tính oxi hóa)
Fe + 2HCl FeCl2 + H2
2Al + 6HCl 2AlCl3 + 3H2
Cu + HCl → không có phản ứng
6.3. Tác dụng với oxit bazo và bazo
Sản phẩm tạo muối và nước
NaOH + HCl → NaCl + H2 O
CuO + 2HCl CuCl2 + H2 O
Fe2 O3 + 6HCl 2FeCl3 + 3H2 O
6.4. Tác dụng với muối (theo điều kiện phản ứng trao đổi)
CaCO3 + 2HCl → CaCl2 + H2O + CO2↑
AgNO3 + HCl → AgCl↓ + HNO3
(dùng để nhận biết gốc clorua )
Ngoài tính chất đặc trưng là axit , dung dịch axit HCl đặc còn thể hiện vai trò chất khử khi tác dụng chất oxi hoá mạnh như KMnO4, MnO2, K2 Cr2O7, MnO2, KClO3 ……
4HCl + MnO2 MnCl2 + Cl + 2H2 O
K2 Cr2 O7 + 14HCl → 3Cl2 + 2KCl + 2CrCl3 + 7H2 O
Hỗn hợp 3 thể tích HCl và 1 thể tích HNO3 đặc được gọi là hỗn hợp nước cường toan ( cường thuỷ) có khả năng hoà tan được Au ( vàng)
3HCl + HNO3 → 2Cl + NOCl + 2H2O
NOCl → NO + Cl
Au + 3Cl → AuCl3
7. Câu hỏi vận dụng liên quan
Câu 1. Dãy chất nào sau đây phản ứng được với dung dịch HCl
A. Mg(OH)2, Fe, CaO
B. Cu(OH)2, Cu, ZnO
C. NaOH, Al, ZnO
D. KOH, Fe, CO2
Lời giải:
Câu 2. Kim loại nào sau đây phản ứng được cả với dung dịch HCl loãng và NaOH
A. Cr
B. Cu
C. Zn
D. Ag
Lời giải:
Câu 3. Cho dãy các bazơ sau: NaOH, Mg(OH)2, Ca(OH)2, Cu(OH)2, Fe(OH)2. Số bazo không tan là:
A. 2
B. 3
C. 4
D. 1
Lời giải:
Câu 4. Dãy các bazo bị nhiệt phân hủy tạo thành oxit bazo
A. Cu(OH)2; Zn(OH)2; Al(OH)3; Fe(OH)2
B. Cu(OH)2; Zn(OH)2; Al(OH)3; NaOH
C. Fe(OH)3; Cu(OH)2; KOH; Fe(OH)2
D. Fe(OH)3; Cu(OH)2; Ca(OH)2; Fe(OH)2
Lời giải:
Câu 5. Có những bazơ sau: Cu(OH)2, NaOH, Ba(OH)2, Mg(OH)2, Fe(OH)3, LiOH, KOH. Hãy cho biết số bazo bị nhiệt phân hủy là:
A. 3
B. 4
C. 5
D. 2
Lời giải:

