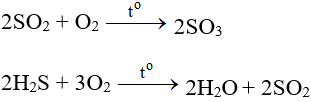Phản ứng SO2 + O2 → SO3
1. Phương trình phản ứng
2SO2 + O2 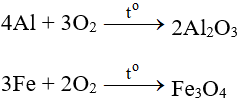
2. Điều kiện để phản ứng SO2 ra SO3
Oxi hóa SO2 bằng khí oxi hoặc không khí dư ở nhiệt độ 450 – 500oC, chất xúc tác vanađi (V) oxit V2O5.
3. Tính chất hóa học của SO2
Là chất khí không màu, nặng hơn không khí, mùi hắc, độc, tan và tác dụng được với nước.
* SO2 là oxit axit
3.1 Lưu huỳnh đioxit Tác dụng với nước
SO2+ H2O ⇋ H2SO3
3.2. Lưu huỳnh đioxit Tác dụng với dung dịch bazơ
(có thể tạo thành 2 loại muối sunfit và hiđrosunfit)
SO2 + NaOH → NaHSO3
SO2 + 2NaOH → Na2SO3 + H2O
3.3. Lưu huỳnh đioxit Tác dụng với oxit bazơ → muối
SO2 + CaO → CaSO3
* SO2 vừa là chất khử, vừa là chất oxi hóa (do S trong SO2 có mức oxi hóa trung gian +4)
3.4. Lưu huỳnh đioxit là chất oxi hóa
SO2 + 2H2S → 3S + 2H2O
3.5. Lưu huỳnh đioxit là chất khử
2SO2 + O2 ⇋ 2SO3 (V2O5, 4500C)
Cl2 + SO2 + 2H2O → H2SO4 + 2HCl
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
SO2 + Br2+ 2H2O → H2SO4 + 2HBr
4. Tính chất hóa học của O2
– Khi tham gia phản ứng, nguyên tử O dễ dàng nhận thêm 2e. Nguyên tử oxi có độ âm điện lớn (3,44), chỉ kém flo (3,98).
– Do vậy, oxi là nguyên tố phi kim hoạt động hoá học, có tính oxi hoá mạnh. Trong các hợp chất (trừ hợp chất với flo), nguyên tố oxi có số oxi hoá là -2.
– Oxi tác dụng với hầu hết các kim loại (trừ Au, Pt, …) và các phi kim (trừ halogen). Oxi tác dụng với nhiều hợp chất vô cơ và hữu cơ.
4.1. Tác dụng với kim loại
Tác dụng với hầu hết kim loại (trừ Au và Pt), cần có to tạo oxit:
4.2. Tác dụng với phi kim
Tác dụng với hầu hết phi kim (trừ halogen), cần có to tạo oxit:
ĐB: Tác dụng với H2 nổ mạnh theo tỉ lệ 2:1 về số mol:
4.3. Tác dụng với hợp chất
– Tác dụng với các chất có tính khử:
– Tác dụng với các chất hữu cơ:
5. Bài tập vận dụng
Câu 1. Khí CO2 có lẫn SO2. Trong các hóa chất sau:
(1) dung dịch NaOH;
(2) dung dịch Br2;
(3) dung dịch KMnO4;
(4) dung dịch Na2SO3;
(5) nước vôi trong;
(6) khí O2.
Có bao nhiêu hóa chất có thể sử dụng để loại bỏ khí SO2 ra khỏi CO2.
A. 4
B. 5
C. 3
D. 2
Lời giải:
Đáp án: C
Giải thích:
Các hóa chất có thể dùng để loại khí SO2 ra khỏi CO2 là:
(2) dung dịch Br2;
(3) dung dịch KMnO4;
(4) dung dịch Na2SO3
Câu 2. Trong các câu sau đây, câu nào sai?
A. Khi sục SO2 vào dung dịch NaOH theo tỉ lệ 1< nNaOH/nSO2< 2 thu được hỗn hợp 2 muối Na2SO3và NaHSO3.
B. Sục SO2 vào dung dịch K2CO3 tạo khí CO2.
C. SO2 vừa có tính oxi hóa, vừa có tính khử.
D. SO2 làm mất màu dung dịch brom.
Lời giải:
Đáp án: B
Giải thích:
Câu sai là: Sục SO2vào dung dịch K2CO3 tạo khí CO2. SO2 không đẩy được CO2 ra khỏi dung dịch
Câu 3. Khí CO2 có lẫn SO2. Trong các hóa chất sau:
(1) dung dịch NaOH;
(2) dung dịch Br2;
(3) dung dịch KMnO4;
(4) dung dịch Na2SO3;
(5) nước vôi trong;
(6) khí O2.
Có bao nhiêu hóa chất có thể sử dụng để loại bỏ khí SO2 ra khỏi CO2.
A. 4
B. 5
C. 3
D. 2
Lời giải:
Đáp án: C
Giải thích:
Các hóa chất có thể dùng để loại khí SO2ra khỏi CO2 là:
(2) dung dịch Br2;
Có khí SO2làm mất màu dung dịch Brom
SO2 + Br2 + 2H2O → 2HBr + H2SO4
(3) dung dịch KMnO4;
5SO2 + 2KMnO4 + 2H2O → 2MnSO4 + K2SO4 + 2H2SO4
(4) dung dịch Na2SO3
Na2SO3 + 2CO2 + H2O → 2NaHCO3 + SO2
Câu 4. Khi làm thí nghiệm với H2SO4 đặc, nóng thường sinh ra khí SO2. Để hạn chế tốt nhất khí SO2 thoát ra gây ô nhiễm môi trường, người ta nút ống nghiệm bằng bông tẩm dung dịch nào sau đây:
A. cồn.
B. muối ăn.
C. xút.
D. giấm ăn.
Lời giải:
Đáp án: C
Giải thích:
Để hạn chế khí SO2 bay ra, người ta sử dụng bông tẩm xút vì xút có khả năng phản ứng:
SO2 + 2NaOH → Na2SO3 + H2O
Câu 5. SO2 vừa có tính oxi hóa, vừa có tính khử vì trong phân tử SO2
A. S có mức oxi hóa trung gian.
B. S có mức oxi hóa cao nhất.
C. S có mức oxi hóa thấp nhất.
D. S còn có một đôi electron tự do.
Lời giải:
Đáp án: A
Giải thích: